SARS-CoV-2 を正確かつ高感度に検出するためのマルチプレックス 1 ステップ RT-qPCR アッセイ
Andrea Corr, BSc and Matteo Beretta, PhD
Introduction
新型コロナウイルス感染症(COVID-19)の出現と急速な拡大は、世界中の国々や人々にとって大きな健康上の脅威となっています。2019年12月に中国武漢で発生したこの流行は、2020年3月11日に世界保健機関(WHO)によってパンデミックと宣言されました。本稿執筆時点で、世界中で51,718,344件の症例が報告され、1,276,527人が死亡しています。[1]
COVID-19の原因物質は、コウモリに由来すると考えられているベータコロナウイルスである、感染力の非常に強い重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2、以前は2019-nCoV)です。このウイルスは、主に呼吸器からの飛沫との直接接触によってヒトからヒトへ伝染します。
コロナウイルスは、エンベロープを持つ一本鎖プラス鎖RNAウイルスで、ヒトや動物に感染します。SARS-CoV-2ウイルス(図1参照)は、肺、心臓、腎臓、血管、胃腸組織に広く発現しているACE2膜貫通受容体に結合するスパイクタンパク質を介してヒト細胞に感染します。
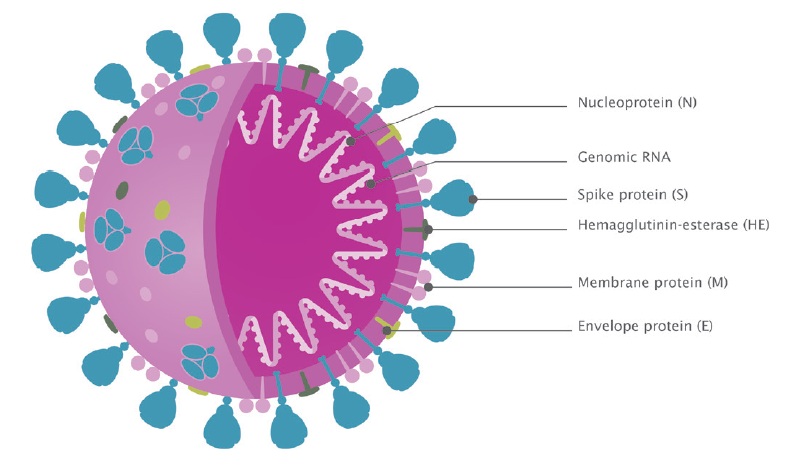
図1:SARS-CoV-2の構造
SARS-CoV-2ゲノムは29,903ヌクレオチドで構成されています。[2] 最初の3分の2はORF1aとORF1bという2つのオープンリーディングフレームで構成され、ウイルスゲノムの複製と校正を助ける16の非構造タンパク質(NSP)をコードしています(図2を参照)。NSP12は高度に保存されたRNA依存性RNAポリメラーゼ(RdRp)をコードしています。ゲノムの残りの3分の1は、スパイク(S)タンパク質、膜(M)タンパク質、エンベロープ(E)タンパク質、ヌクレオカプシド(N)タンパク質の4つの構造タンパク質の遺伝子と、宿主防御を阻害するアクセサリタンパク質の8つの遺伝子で構成されています。
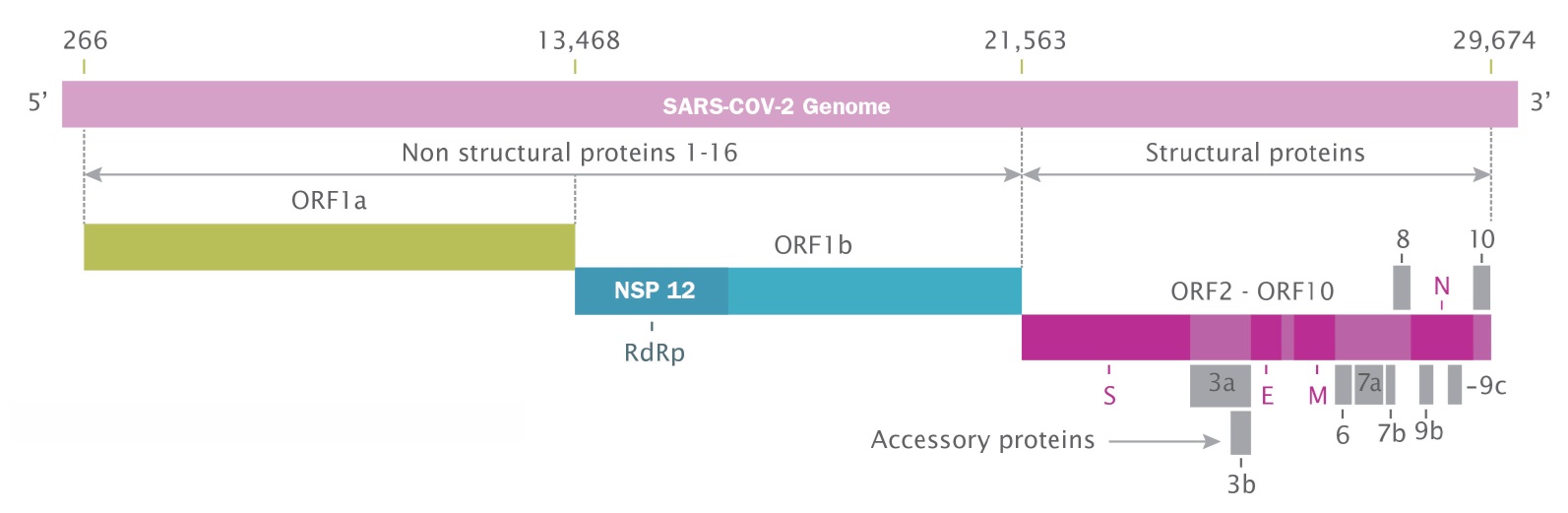
図2:SARS-CoV-2ゲノムの構成
COVID-19 のような新しいウイルス性疾患の出現により、標的ウイルスを大規模に検出および特定するための迅速な方法の必要性が浮き彫りになっています。大規模検査と強力で効果的な追跡がパンデミックの制御の鍵となります。検査に関しては、患者の鼻咽頭スワブサンプルと、専門の臨床封じ込めラボでの RT-qPCR ベースの検出の組み合わせがゴールドスタンダードと考えられています。
Multiplex testing
RT-qPCR ベースの SARS-CoV-2 の検出は、単一のターゲット配列を単一のウェルで増幅するシングルプレックス、またはスペクトル的に異なる蛍光体で標識されたプローブと組み合わせて複数のプライマーペアを使用して複数のターゲットを同時に増幅するマルチプレックスで実行できます。
寒い時期に実施される SARS-CoV-2 検査は、SARS-CoV-2 をインフルエンザ A 型、インフルエンザ B 型、RS ウイルス (RSV) などの他の一般的な季節性ウイルスと区別するために設計された多重呼吸器パネル検査の一部となる可能性が高いです。多重アッセイは、時間、労力、試薬の使用を大幅に節約できる可能性があるが、1 回の RT-qPCR 反応でターゲットの数が増えるため、最適化がはるかに困難になります。
このアプリケーション ノートでは、SARS-CoV-2 検出のための迅速かつ高感度のマルチプレックス RT-qPCR アッセイについて詳しく説明します。このアプリケーション ノートは、COVID-19 の効果的なハイスループット診断テストの開発に貢献し、その取り組みをサポートするように設計されています。
Method
PCR Biosystems 社は最近、配列特異的プローブを使用した1ステップ RT-qPCR によるウイルス RNA の検出用 qPCRBIO Probe 1-Step Virus Detect を発表しました。このキットは、高濃度4倍ミックスと UltraScript 逆転写酵素で最適化されています。合成ウイルス RNA をテンプレートとして使用し、WHO/Charité-Berlin プロトコル[3]および米国疾病予防管理センター(CDC、米国アトランタ)プロトコル[4]で概説されている標的配列を使用した、マルチプレックスでの SARS-CoV-2 の定性検出の実験条件について説明します。科学者の時間とリソースを節約するため、逆転写時間と温度、プライマーとプローブの濃度などの RT-qPCR 変数を調査しました。ここでは、SARS-CoV-2 ルチプレックスアッセイを最初からうまく機能させるための最適化された実験セットアップの概要を示します。
Target sequences
私たちは 4 つのターゲット配列 (表 1 を参照) を検査しました。WHO/Charité-Berlin によって記述された RdRp および E 遺伝子ターゲット、CDC によって記述された N2 ターゲット、およびヒト抽出コントロール RPP30 です。RPP30 は RNAse P サブユニット P30 をコードし、診断キットによく含まれています。プライマーとプローブは Biolegio および Integrated DNA Technologies から入手しました。
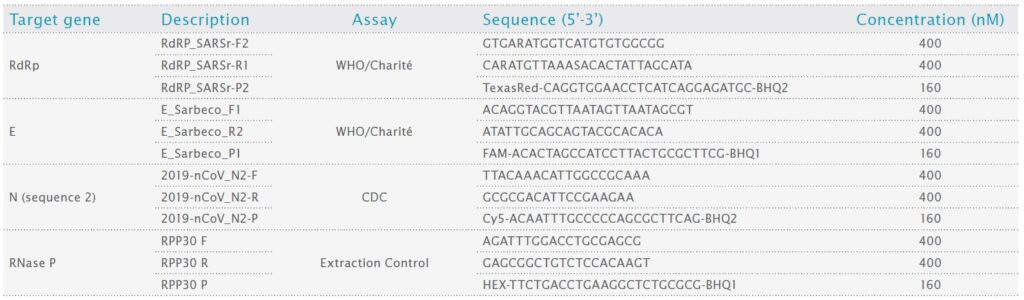
表1:SARS-CoV-2とヒトRNase Pプライマーおよびプローブ配列
RNA template
ウイルスゲノム (ATCC、カタログ番号 VR-3276SD) の希釈は、PCR グレード dH20 を使用して Qiagen QIAgility ロボットで実施しました。5 回の連続 10 倍 RNA ウイルス希釈は、5μL で 40,000 コピーから始めて、5μL で 4 コピーまで減らし、4 回繰り返して実施しました。テンプレートなしのコントロール (NTC) も 4 回繰り返して実施しました。
ヒト肺 RNA (ThermoFisher、カタログ番号 AM7968) の希釈は、Qiagen QIAgility ロボットで PCR グレードの dH20 とウイルス RNA を使用して実行されました。ヒト肺RNAの10倍希釈は、5μL中250ngから始めて5μL中25pgまで4回繰り返し実施しました。NTCも4回繰り返し実施しました。
Reaction setup
PCR マスター ミックスは、表 2 に示すように Qiagen QIAgility ロボットを使用して、最終反応容量 20μL で調製されました。
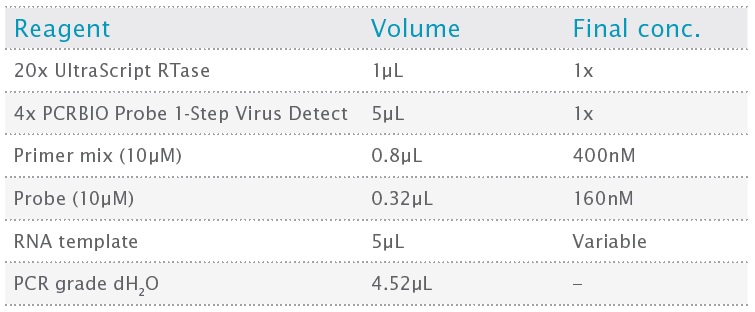
表2:反応のセットアップ
4 セットのプライマー ペア (F+R) を混合して、各オリゴヌクレオチドの最終濃度が 10 μM になるようにしました (例: 100 μM のプライマーの 8 つのストックのそれぞれに 10 μL、PCR グレードの dH2O 20 μL)。同様に、4 つのプローブを混合して、各最終濃度が 10 μM になるようにしました (例: 100 μM のプローブの 4 つのストックのそれぞれに 10 μL、PCR グレードの dH2O 60 μL)。
Cycling conditions
PCR サイクリングは Bio-Rad CFX96 Touch™ を使用して実行されました。最適な RT-qPCR プログラムを表 3 に示します。
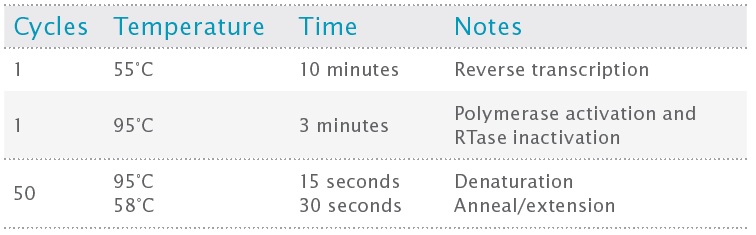
表3:サイクリング条件
Results
SARS-CoV-2 ウイルスターゲットのすべての希釈度は、この 4 プレックス RT-qPCR プログラムで高い効率値で検出されました (図 3 および表 4 を参照)。平均最初の Ct は 40,000 コピーで 24.74、平均最終 Ct は 4 コピーで 39.16 でした。qPCRBIO Probe 1-Step Virus Detect は、SARS-CoV-2 ターゲットをマルチプレックスで検出するために使用でき、高い特異性と感度で、20μL 反応あたり 4 コピー (μL あたり 0.8 コピー) までテストされています。
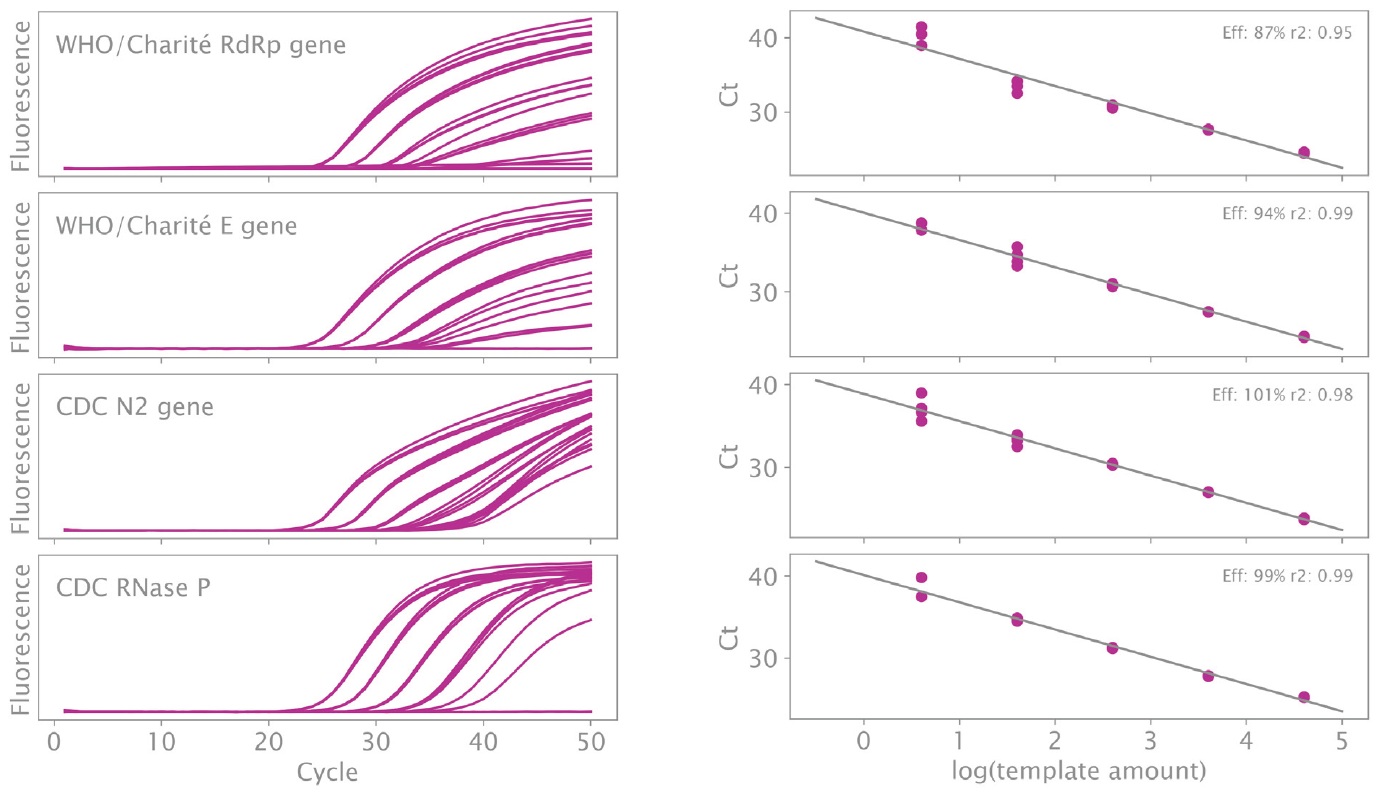
図1:qPCRBIO Probe 1-Step Virus Detect を使用した SARS-CoV-2 核酸の多重検出
qPCRBIO Probe 1-Step Virus Detect を4回使用して、SARS-CoV-2 RdRp、E および N 遺伝子とヒト RNase P 遺伝子を4重に増幅しました。増幅曲線は左側に、効率は右側に示されています。合成ウイルス RNA テンプレートの 5 つの連続希釈液を使用しました。これは、SARS-CoV-2 ゲノムの 40,000、4,000、400、40、および 4 コピーに相当します。ウイルスゲノム溶液では、250 ng から 25 pg までのヒト肺 RNA テンプレートの 5 つの連続希釈液を使用しました。総反応容量は 20 μL でした。RdRp-P2 プローブは Texas Red、E 遺伝子プローブは FAM、N2 プローブは Cy5、RNase P プローブは HEX でラベル付けしました。使用したサイクリング条件は表 3 に示されています。
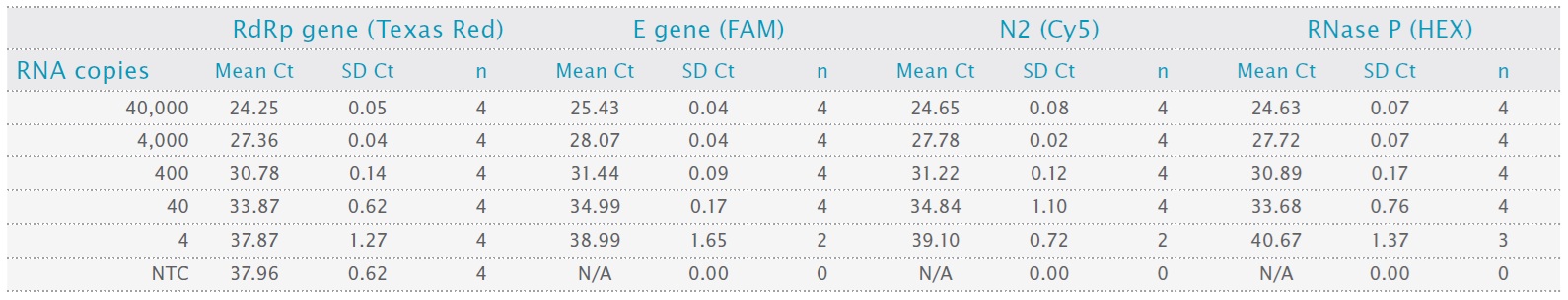
表4:平均Ct値と標準偏差値
この表は、qPCRBIO Probe 1-Step Virus Detect を使用して SARS-CoV-2 RdRp、E、N 遺伝子およびヒト RNase P 遺伝子を増幅したときに得られた平均 Ct 値と標準偏差 (SD Ct) 値を示しています。n は、正の増幅を示す反復回数 (4 回中) を示します。
Discussion
RT-qPCR 検査は、正しく実施すれば、感度と特異度が非常に高く、SARS-Cov-2 ゲノム物質を検出することで COVID-19 診断のゴールド スタンダードとなります。ただし、「陽性」PCR 結果はウイルス RNA の検出のみを反映しており、必ずしも生存ウイルスの存在を示すものではないことに留意する必要があります。この検査の感度は、患者から非常に微量のウイルス RNA を検出できるほどです。ウイルスの拡散を抑えるには、これらの低陽性患者をできるだけ早く検出することが重要です。
マルチプレックス検査では、1 回の qPCR 反応で複数の呼吸器ウイルス ターゲットを検査できるため、サンプル処理に関する貴重な時間を節約できます。マルチプレックス検査により、各患者サンプルに関するより多くの情報が臨床医に提供されます。マルチプレックス RT-qPCR 反応を最適化することは困難で、貴重な時間がかかる可能性があるため、このアプリケーション ノートでは、感度の高い結果につながる RT-qPCR パラメータとマスター ミックスの提案について詳しく説明します。RT-qPCR の感度は、効果的な鼻咽頭スワブ サンプリング、ウイルス不活化バッファー内でのウイルスの通過温度、その後の検査用ウイルス サンプルの品質などの外部要因によって影響を受けます。このアプリケーション ノートでは、qPCRBIO Probe 1-Step Virus Detect の合成 RNA の検出に関する感度のみを説明し、抽出された患者スワブについては説明しません。
2020年6月にFDAが提案したアイデアである患者サンプルのプール[5]は、無症状の患者のスクリーニングに役立ち、多数の陰性患者サンプルを迅速に無視できるため価値があります。その後の検査と調査は、陽性と判定されたプールされたサンプルのみに集中できます。
本稿執筆時点では、R 値は再び上昇傾向にあります。このウイルスが永久に人口に残るのか、あるいは季節性インフルエンザの場合のように人々が繰り返しワクチン接種を受けることになるのかは不明です。しかし、ワクチン接種がない場合は、迅速かつ効率的な診断が、このウイルスの拡散を抑制し、今後数か月から数年にわたって世界的な社会的、経済的影響を軽減する鍵となります。
Product use
qPCRBIO Probe 1-Step Virus Detect 単体では診断結果は得られず、研究用途のみに提供されます。該当する国の法律で許可されている場合、分子診断アッセイのコンポーネントとして使用するのに適しています。
References
- COVID-19 Dashboard by the Centre for Systems Science and Engineering at Johns Hopkins University accessed 11th November 2020 (https://coronavirus.jhu.edu/map.html)
- Severe acute respiratory syndrome coronavirus 2 isolate Wuhan-Hu-1, complete genome (https://www.ncbi.nlm.nih.gov/nuccore/MN908947)
- Diagnostic detection of 2019-nCoV by real-time RT-PCR (https://www.who.int/docs/default-source/coronaviruse/protocol-v2-1.pdf)
- Research Use Only 2019-Novel Coronavirus (2019-nCoV) Real-time RT-PCR Primers and Probes (https://www.cdc.gov/coronavirus/2019-ncov/lab/rt-pcr-panel-primer-probes.html)
- Coronavirus (COVID-19) Update: Facilitating Diagnostic Test Availability for Asymptomatic Testing and Sample Pooling, (https://www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-facilitating-diagnostic-test-availabilityasymptomatic-testing-and)
